Mit dem Beprogramm Wenn die FDA die Effizienz von Zulassungsverfahren (z. B. 510 (k)) durch Digitalisierung erhöhen möchte. Der Johner -Institut arbeitet mit der FDA in der Weiterentwicklung von Estar zusammen.
In diesem Artikel werden Sie herausfinden, wie vorwärts diesen Ansatz aussieht und ob Sie teilnehmen sollten oder müssen.
1. Was ist das Estar -Programm?
Mit dem Estar -Programm können die Hersteller von Medizinprodukten ihre Zulassungsdokumente über ein interaktives PDF an die FDA übermitteln.
a) Interaktivität
Interaktivität hat mehrere Aspekte.
Integrierter Fehlertest
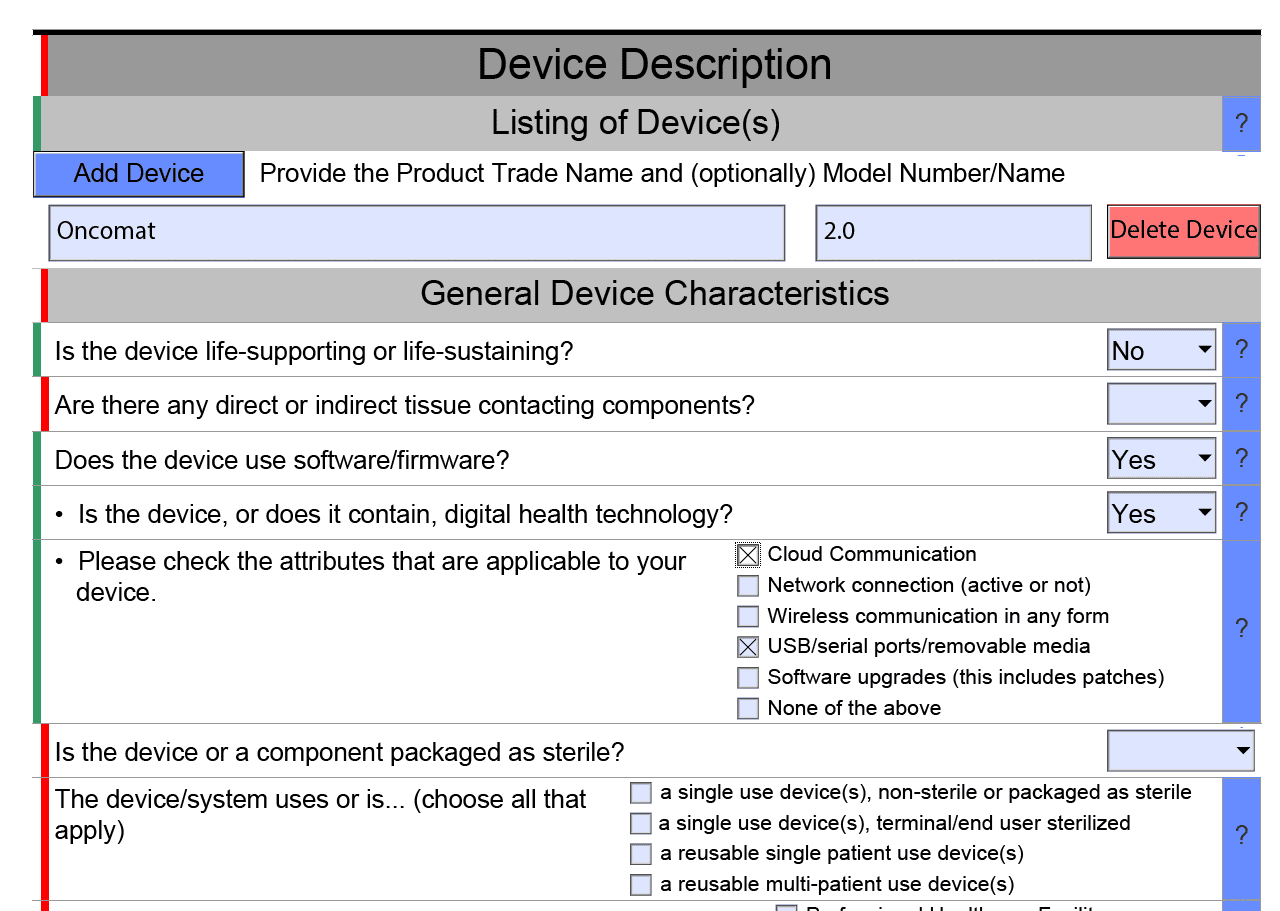
Die PDF markiert Bereiche, in denen Daten offensichtlich immer noch Fehler in rotem und korrekten Bereichen in Grün enthalten (siehe Abb. 1).
Automatisierte Eingabe und Versteck in Bereichen
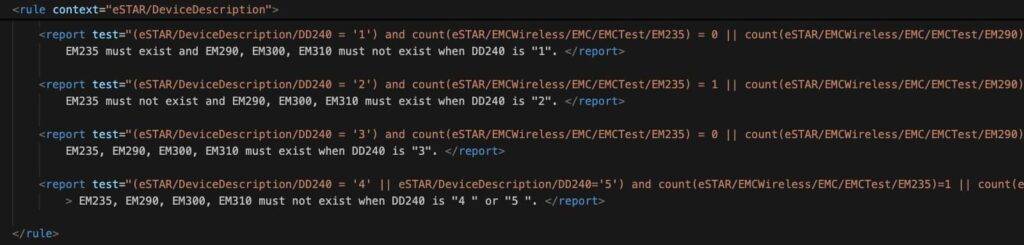
Das interaktive Dokument verbirgt je nach Auswahl Bereiche oder aus. Beispielsweise zeigt das Dokument automatisch Details zu den Softwaredokumenten an, wenn Sie auswählen, dass das Produkt Software enthält oder eine eigenständige Software ist (siehe Abb. 1). Die FDA definiert diese Logik für eingehende und versteckte Schematron-Dateien (siehe Abb. 2).
Integration von Anhängen
Mit dem PDF können Anhänge angebracht werden. Aus der Sicht der FDA müssen diese Anhänge sogar hinzugefügt werden. Es gibt keine Einschränkung des Datenformates. Nur die Größe des resultierenden PDF -Dokuments ist auf 1 GB begrenzt (siehe Abb. 3).

Möglichkeiten zum Import und Exportieren
Alle Daten können mit Ausnahme der Anhänge über das PDF aus XML importiert und gemäß XML exportiert werden.
b) Elektronische Einreichung
In der Zwischenzeit erfolgt die Einreichung nicht mehr auf einem physischen Datenträger, sondern elektronisch. Abhängig vom verantwortlichen FDA-Zentrum reichen die Hersteller im CDRH-Portal oder über das ESG-Gateway für CBER-bezogene Einreichungen.
c) Estar gegen Ecopy
Tatsächlich repräsentiert das ESTAR -Programm nach dem Programm für ECOPY/ESUBMITTER die nächste Evolution in der Digitalisierung. Im ECOPY/ESUBMITTER -Programm gab die FDA nur “nur” die Formatierung der elektronischen Einreichungsdateien, an die die Hersteller festhalten müssen. Es gibt keine vorgegebene Struktur der Dokumente selbst oder sogar strukturierte Daten wie das ESTAR -Programm mit dem ECOPY/ESUBMITTER -Programm.
Wenn Sie mehr über die Geschichte dieser beiden Programme erfahren und einen Vergleich wünschen, wird ein Blick auf dieses Leitfadendokument empfohlen.
2. Wer kann das Estar -Programm verwenden oder kann?
Offensichtlich sollte das ESTAR -Programm die Hersteller von Medizinprodukten beim Zusammenstellen und Einreichen von Genehmigungsdokumenten schneller und besserer Qualität unterstützen. Es wendet sich jedoch nicht an alle Hersteller zu und eignet sich nicht für alle Zulassungsverfahren.
Das ESTAR -Programm gilt nur für:
Die Teilnahme am Estar -Programm ist explizit freiwillig. Hersteller und Produkte, für die das Verfahren anwendbar ist, müssen jedoch nicht teilnehmen.
510 (k) Verfahren sind ausgeschlossen. Hier ist die Teilnahme am Estar -Programm obligatorisch.
3. Wie hilft das Estar -Programm?
Das ESTAR -Programm kommt den Herstellern sowie der FDA zugute.
a) Dokumente in besserer Qualität
Die FDA erhält die Dokumente in höherer Qualität, da die PDF den Herstellern hilft, offensichtliche Fehler wie fehlende Informationen oder Tippfehler zu vermeiden (z. B. für Produktcodes). Dropdown-Listen und Überprüfungen des Inhalts tragen beispielsweise zur Vollständigkeit und Konsistenz bei.
b) mehr Sicherheit
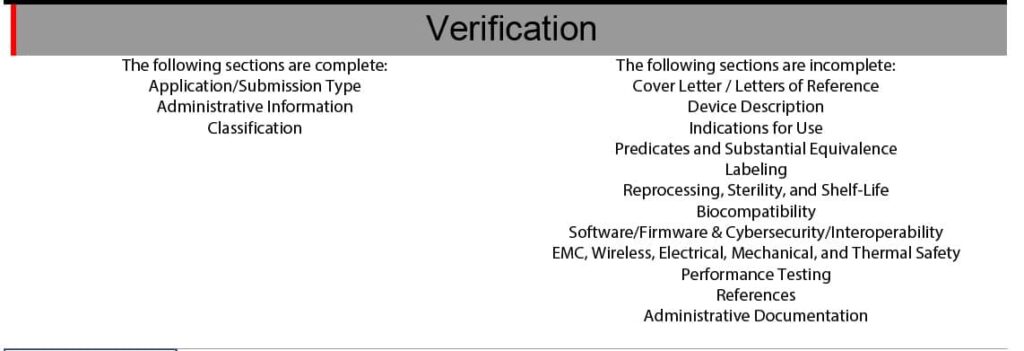
Die PDF überprüfte unvollständige oder fehlende Informationen sowohl auf der Ebene des einzelnen Datums als auch auf der Ebene des gesamten Dokuments (siehe Abb. 3).
c) weniger Anstrengung
Die Hersteller und die FDA retten sich die RTA -Korrekturschleife. Der Rest des Prozesses bleibt jedoch unverändert:
Der Rest einer Überprüfung von 510 (k) wird gemäß der FDA -Leitlinie „Das 510 (k) -Programm: Bewertung erheblicher Äquivalenz in Prämarket -Benachrichtigungen durchgeführt [510(k)]”Nach den in 21 CFR 807 -Unterabschnitt E identifizierten Verfahren. Eine De -novo -Überprüfung erfolgt gemäß der FDA -Leitlinie„ De -novo -Klassifizierungsprozess (Bewertung der automatischen Klasse -III -Bezeichnung), nach den in 21 CFR 860 identifizierten Verfahren, Abschnitt D.
Die FDA muss Inhalte mithilfe einer Kopie und Paste nicht an ihre eigenen Systeme übergeben. Dies spart auch Anstrengung.
Darüber hinaus findet die Behörde die Dokumente schneller, da der Zugriff auf den Inhalt und die Anhänge direkt über das PDF -Dokument möglich ist und die Hersteller gezwungen sind, die von der FDA angegebenen Anhänge in der von der FDA festgelegten Struktur zu kompilieren. Dies rettet auch die Autorität. Sie stimmt jedoch keine kürzere Verarbeitungszeit zu.
4. Bewertung des Estar -Programms
a) positiv
Mit diesem Programm unterstützt die FDA die Hersteller, vollständige, konsistente und korrekte Dokumente zusammenzustellen.
Durch die Automatisierung vieler vorläufiger Prüfungen profitiert auch die Behörde selbst. Dies wiederum kommt den Herstellern zugute, da die Genehmigungsprozesse schneller und insbesondere unnötige Iterationsschleifen (einschließlich RTA -Test) erfolgen.
Die Struktur des PDF -Dokuments (siehe Abb. 4) und die Verteilung der Anhänge gibt den Herstellern wertvolle Vorschläge, um ihre eigenen Dokumente zu strukturieren. Dies gilt sowohl auf der Ebene der Verzeichnisse als auch auf den Dokumenten selbst.

b) Kritik
Die Möglichkeit eines XML -Imports kann bestenfalls eine Übergangstechnologie sein, um die Informationen von vorhandenen Systemen in das FDA -PDF -Dokument zu übertragen. Dies ist besser als ein manuelles Kopier und ein Paste, aber kein Ersatz für eine API.
Die FDA legt die (Struktur der) erwarteten Anhänge an. Dabei zwingt es die Hersteller, ihre Dokumente fda-speziell zusammenzustellen. Dies führt zu der üblichen Fleißung von Regulierungsunternehmen. Aufgaben, die eine vollständige Digitalisierung der Prozesse überflüssig machen könnten und sollten.
c) Bewertung und Aussicht
Mit dem Estar -Programm ist die FDA ein klarer Schritt weiter als in vielen benannten Bereichen mit ihren “Antragsformularen”. Diese können oft weder mit der Funktionalität noch mit der Benutzerfreundlichkeit und Interoperabilität Schritt halten (XML -Import und Experte).
Die interaktive PDF ist Software, die wie jede andere Software weiter validiert und weiterentwickelt werden muss. Bisher wurde die FDA sehr schnell aktualisiert. Beispielsweise wurde das neue Leitfaden für Software mit der Unterscheidung gemäß “Basic -Dokumentation” und “Enhanced Dokumentation” implementiert.
5. Schlussfolgerung
a) Zusammenfassung
Mit dem Estar -Programm macht die FDA den nächsten Schritt zur Digitalisierung der Genehmigungsverfahren. Es treibt dies nach oben, was mit einem Dokument und einem PDF-basierten Ansatz erreicht werden kann.
Die Interaktivität der PDF -Dokumente mit integrierter Anwendungslogik und einer Mischung strukturierter Daten und Anhänge zeigt an, was mit einer vollständig automatisierten Aufzeichnung und Überprüfung von Registrierungsdaten möglich wäre.
Bis dahin müssen die Hersteller mit Dokumenten arbeiten und die folgenden Richtlinien beobachten:
Das Johner -Institut unterstützt Hersteller und benannte Bereiche in der digitalen Transformation. Interesse? Dann setze dich an!
Versionshistorie:
- 2025-10-02: Am Anfang ein Satz zum “De-Novo-Inhalt”, der zu Beginn ergänzt ist.
- 2024-10-15: Hinweis zur obligatorischen Verwendung von Estar für De-novo-Anfragen vom 1. Oktober 2025 ergänzt
- 2024-08-20: Bewertungen, die in das neue Kapitel 4. Nummerierung konsequent implementiert wurde. Einführung hinzugefügt. Kapitel 1.a) neu gestaltet und durch das Bild der Schematrone -Datei (Abb. 2) überarbeitet und hinzugefügt.
- 2023-09-15: Informationen zur elektronischen Einreichung und Verfügbarkeit von Estar für Kombinationsprodukte ergänzt
- 2022-09-23: Anmerkungen zum neuen Estar-Leitfaden-Dokument ergänzt
Ähnliche Beiträge
Automotive
Game Center
Game News
Review Film
Berita Terkini
Berita Terkini
Berita Terkini
review anime