Laut ISO im Jahr 14971 ist ein Restrisiko das “Risiko, das nach Maßnahmen zur Einstellung von Risiken bestehen”. Aber welche Restrisiken sind akzeptabel? Dies erschwert viele Hersteller von Medizinprodukten.
Lesen Sie hier, wie Sie zu belastbaren Akzeptanzkriterien für das Restrisiko kommen. Diese Zahlen können für Sie nützlich sein.
1. restiscis: die Grundlagen
A) Kontext
Medizinprodukte und IVD decken Risiken ab, die Hersteller durch geeignete Maßnahmen so weit wie möglich reduzieren müssen.
Ein Defibrillator kann versehentlich ausgelöst werden und zum Schaden des Patienten führen, z. B. sein Herz. Die Kombination von Schweregrad und Wahrscheinlichkeit dieses Schadens ist das Risiko.
Wenn der Hersteller den Defibrillator so entwirft, dass die Benutzer zwei Hände zum Auslösen benötigen, senkt er die Wahrscheinlichkeit einer zufälligen Auslöschung und damit das Risiko.
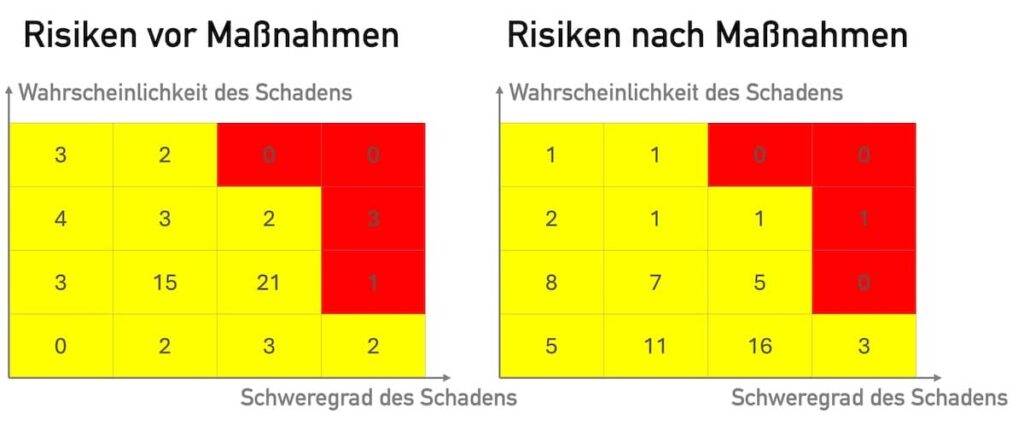
b) Ein-resistenter Risiko im Vergleich zu Gesamtrisikorisiko
Wenn der Hersteller beschließt, im Falle eines Risikos keine weiteren Maßnahmen durchzuführen, entspricht das Risiko gemäß den ergriffenen Maßnahmen dem individuellen Ruherisiko.
Analog entspricht die Gesamtbeschränkung des Produkts dem Risiko nach allen getroffenen Maßnahmen.
2. REST -Risiko: regulatorische Anforderungen
a) Anforderungen von ISO 14971
Die ISO 14971 -Anforderungen der Hersteller, jedes einzelne Risiko für die Akzeptanz zu bewerten. Diese Einschätzung muss auf den im Risikomanagementplan festgelegten Kriterien beruhen.
Die Hersteller sind auch verpflichtet, sicherzustellen, dass die Vorteile des Produkts die Gesamtbeschränkung überwiegt.
Die Hersteller müssen auch entscheiden, welche verbleibenden Risiken sie z. B. In einer Anweisung offenlegen.
Immerhin fordert der Standard, dass die verbleibenden Risiken und ihre Akzeptanz kontinuierlich bewertet werden, wenn die Produkte auf dem Markt sind.
b) Mdr
Der MDR verpflichtet die Hersteller, sowohl den einzelnen Rest des Restes als auch das Gesamtrisikorisiko zu minimieren:
In der Reihenfolge des Risikos des Risikos zielt das Risikomanagement der Hersteller darauf ab, dass sowohl das verbleibende Risiko mit jedem einzelnen Gefahren als auch das Gesamtrisiko als akzeptabel eingestuft werden.
Mdr, Anhang I, 4.
Der MDR fordert zwei Orte, an denen die verbleibenden Risiken in den Gebrauchsanweisungen offengelegt werden:
Die Hersteller unterrichten Benutzer über Restrisiken.
Mdr, Anhang I, 4.
Die Verwendungsanweisungen enthält alle folgenden Informationen:
g) Restrisiken, Kontraindikationen und alle unerwünschten Nebenwirkungen, einschließlich der Informationen, die dem Patienten in diesem Zusammenhang informiert werden sollen;
Mdr, Anhang I, 23,4
3. Welche Restrisiken sind akzeptabel?
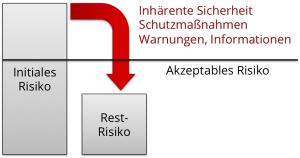
In diesem detaillierten Beitrag zur Risikoakzeptanz wird erläutert, dass ein Risiko nur dann akzeptabel sein kann, wenn der Nutzen höher ist.
Beispiel 1: Restrisiko von Produkten mit potenziell tödlichen Konsequenzen
Ein Strahlungsgerät dient VA zur Behandlung von Krebspatienten. Die Strahlung verursacht jedoch Strahlungsschäden, was wiederum neue Krebs auslösen kann.
Das Risiko dieser strahlungsbedingten, potenziell tödlichen Erkrankung ist nur dann akzeptabel, wenn der Nutzen höher ist. Insbesondere muss die Anzahl der Todesfälle, die mit dem Gerät auftreten, kleiner sein als die Anzahl der Todesfälle, die ohne das Gerät auftreten. „Ohne Gerät“ bedeutet jedoch nicht, dass die Patienten überhaupt nicht behandelt werden, sondern mit der besten Alternative, z. B. ein weiteres Strahlungsgerät, Chemotherapie, eine Operation usw.
Diese Alternativen repräsentieren den Stand der Technik.
Beispiel 2: Restrisiko von Produkten ohne potenziell tödliche Konsequenzen
Dieses Argument gilt nicht für medizinische Geräte, die kein Leben untersparen können. Ein Beispiel ist ein Laufband für die Rehabilitation. Im besten Fall kann das Produkt dazu beitragen, dass die Patienten nach einer Krankheit oder einem Unfall im wahrsten Sinne des Wortes schneller auf den Beinen sind.
Trotzdem können diese Produkte Patienten verursachen:
- Der Patient fällt beispielsweise, weil das Laufband blockiert und mit dem Kopf auf dem Boden trifft.
- Die Isolation eines Kabels bricht; Daher liegt die Netzspannung direkt am Gehäuse und der Patient hat einen elektrischen Schock.
Um zu prüfen, ob ein verbleibendes Risiko akzeptabel ist, gilt der Vergleich der Anzahl der Todesfälle nicht mehr wie im ersten Beispiel. Was zu tun?
Mögliche Kriterien für Risikoakzeptanz
Um zu entscheiden, ob ein verbleibendes Risiko akzeptabel ist, bieten die folgenden Arten von Kriterien an:
- Direkter Vergleich des Nutzens und der Risiken des Produkts und der besten Alternativen, z. B. basierend auf dem
- Anzahl der Toten
- Anzahl der Verletzungen
- Leben
- Stand der Technik: Im zweiten Beispiel würde das verbleibende Risiko durch einen elektrischen Schock akzeptiert, wenn die elektrische Sicherheit dem Stand der Technik entspricht, dh wenn das medizinische Gerät gemäß den IEC 60601-1 entwickelt und hergestellt würde.
- Vergleich mit den normalen Lebensrisiken: In anderen Branchen wie der Luftfahrtindustrie vergleichen Sie die Risiken mit denen des normalen Lebens. Nur wenn das letztere Risiko signifikant höher ist (z. B. mindestens eine Größe), wird ein Restrisiko als akzeptabel bewertet.
3. Tipps zum Umgang mit Restrisiken
Die folgenden Zahlen können nützlich sein, wenn Sie sich für die Akzeptanz eines Restrisikos entscheiden müssen:
- In deutschen Krankenhäusern treten rund 500.000 Infektionen auf (z. B. Wundinfektionen nach Operationen) [Quelle: Charité]. Wenn Ärzte behaupten, dass keine Todesfälle durch ein medizinisches Gerät verursacht werden sollten. Sie können darauf hingewiesen werden, dass zwischen 80.000 und 180.000 Infektionen vermeidbar wären [Quelle].
- 3.000 Patienten sterben jährlich im Krankenhaus an MRSA -Infektionen; Ein dritter wäre vermeidbar [Quelle]. Die Wahrscheinlichkeit, an einem Keim zu sterben, beträgt daher etwa ein Tausend.
- Der ISO 13849-1 verlangt von einem Maschinenbenutzer seltener als alle 107-Te Arbeitsstunde kann einer Veranstaltung mit einer ernsthaften Episode ausgesetzt sein.
- Die Wahrscheinlichkeit, durch einen Autounfall getötet zu werden, beträgt ungefähr 2 × 10-7 pro Fahrstunde oder 2,7 Todesfälle pro Milliarde Person Kilometer [Quelle].
- Die geringste verzeichnete Sterblichkeitsrate hat ungefähr 15-jährige Mädchen: 3,5 × 10-8/H [Quelle S. 130; lesenswert ist das Kapitel 5.2].
Diese Zahlen helfen Ihnen, das Restrisiko mit den Risiken eines normalen Lebens oder den Risiken in einem Krankenhaus zu vergleichen.
4. Schlussfolgerung und Zusammenfassung
Die Hersteller müssen die individuelle Ausrichtung und das Gesamtruhe des Ruhesrisikos jedes Produkts bestimmen und sie anhand der zuvor definierten Kriterien anhand der Akzeptanz bewerten. Unabhängig davon, ob Sie diese Verpflichtung erfüllen, überprüfen Sie die Behörden und werden regelmäßig Stellen für Zulassungsverfahren, Audits und Inspektionen benannt.
Geschichte verändern
- 2025-05-07: Artikel weitgehend neu geschrieben
- 2015-12-14: veröffentlichte die erste Version des Artikels
Ähnliche Beiträge
Automotive
Jasa Import China
Cek Ongkir Cargo
Berita Teknologi
Seputar Teknologi



